Evitando que las «bacterias pesadilla» se conviertan en «brotes pesadilla»
|
A principios de 2015, la expresión «enterobacterias resistentes a los carbapenems» se popularizó cuando un brote de gran repercusión —que incluyó dos muertes— en un hospital de California se asoció a los endoscopios médicos contaminados1. Pero estos patógenos multirresistentes han constituido un problema creciente desde hace al menos una década. Las infecciones por enterobacterias resistentes a los carbapenems se han multiplicado por cinco entre 2008 y 2012, año en el que se extendieron a 48 estados de EE. UU2. En 2012, los Centers for Disease Control and Prevention (CDC) estadounidenses notificaron que aproximadamente el 4 % de los hospitales de cuidados agudos y el 18 % de los hospitales de cuidados agudos a largo plazo de EE. UU. habían notificado al menos un paciente con una infección por enterobacterias resistentes a los carbapenems durante la primera mitad de ese año3. Ahora, en 2017, un estudio de Control de infecciones y epidemiología hospitalaria de 16 centros sanitarios del área de Washington, D.C., notificó una prevalencia sorprendentemente alta: de un 5,2 %4. Esa es solo un área metropolitana de EE. UU., pero está claro que no es un caso aislado. HAGA CLIC AQUÍ para descargar el libro blanco. |
1. Terhune C. Superbug linked to 2 deaths at UCLA hospital; 179 potentially exposed. Los Angeles Times. 2015 Feb 18. Accessed Oct 2017. http://www.latimes.com/business/la-fi-hospital-infections-20150218-story.html
2. Thaden JT, et al. Rising rates of carbapenem-resistant Enterobacteriaceae in community hospitals: a mixed-methods review of epidemiology and microbiology practices in a network of community hospitals in the Southeastern United States. Infect Control Hosp Epidemiol. 2014 Aug;35(8):978-83.
3. CDC. CDC: Action needed now to halt spread of deadly bacteria. Press release. 2013 Mar 5. Accessed Oct 2017. https://www.cdc.gov/media/releases/2013/p0305_deadly_bacteria.html
4. Reuben J, et al; HARP Study Team. Healthcare antibiotic resistance prevalence - DC (HARP-DC): a regional prevalence assessment of carbapenem-resistant Enterobacteriaceae (CRE) in healthcare facilities in Washington, District of Columbia. Infect Control Hosp Epidemiol. 2017 Aug;38(8):921-29.
Pruebas de vigilancia molecular de rutina de enterobacterias resistentes a carbapenem en un entorno de baja prevalencia
Un estudio en el que se evaluaron pacientes con alto riesgo de ser portadores de enterobacterias resistentes a carbapenem (CRE) productoras de carbapenemasa demostró que las pruebas de vigilancia de rutina pueden ser eficaces como guía para los programas de control de infecciones destinados a limitar la propagación de las CRE, incluso en áreas de baja prevalencia.
Si bien la detección precoz de pacientes colonizados con CRE productoras de carbapenemasa es esencial para el control de las infecciones, no existen recomendaciones claras sobre cuándo deben utilizarse métodos moleculares para la vigilancia activa en entornos de baja prevalencia. Este estudio demostró que una prueba molecular rápida es adecuada para las pruebas de vigilancia de rutina de pacientes de alto riesgo, incluso en regiones de baja prevalencia: El estudio demostró que la prueba Xpert® Carba-R de Cepheid tiene una sensibilidad del 100 % y una especificidad del 99,13 % para la detección de CRE productoras de carbapenemasa obtenidas de muestras de hisopo rectal, en comparación con el cultivo cromógeno tras el enriquecimiento.
El estudio se realizó en un hospital en Francia donde la prevalencia de CRE productoras de carbapenemasa es inferior al 1 %. Entre los «pacientes de alto riesgo» se incluían aquellos repatriados de países con una alta prevalencia de CRE o pacientes que habían tenido contacto con un portador conocido de CRE productoras de carbapenemasa. El estudio permitió formar rápidamente cohortes de portadores, lo cual es esencial para (i) prevenir los brotes y (ii) reducir el impacto social y el coste de las medidas de control de infecciones implementadas empíricamente para los pacientes de alto riesgo, que acaban teniendo resultados negativos para la colonización con CRE productoras de carbapenemasa.
El informe de los resultados se publicó en International Journal of Antimicrobial Agents.
Este estudio demostró que la prueba Xpert® Carba-R es adecuada para las pruebas rápidas de vigilancia de pacientes de alto riesgo, incluso en entornos de baja prevalencia»
Referencia:
Hoyos-Mallecot et al. Int J Antimicrob Agents 49 (6), 774-777. 2017 Apr 12.
Global Laboratory Initiative describe un protocolo para detectar casos activos y precoces de TB
Los laboratorios desempeñan un papel esencial en la identificación de los casos activos y precoces de tuberculosis (TB), lo cual es un aspecto clave para erradicar la enfermedad en todo el mundo. Con el fin de cumplir con los objetivos de la OMS para la prevención de la transmisión de la TB y la mejora de la atención al paciente, Global Laboratory Initiative (GLI) y los expertos de la European Tuberculosis Laboratory Initiative (región europea de la OMS) recomiendan la realización de pruebas rápidas de casos sospechosos de tuberculosis con pruebas diagnósticas moleculares sensibles. Ambos grupos de expertos mundiales recomiendan el uso de Xpert MTB/RIF de Cepheid como prueba de primera línea, en lugar de la microscopía de frotis o ensayos de sonda lineal, junto con métodos basados en cultivo para las pruebas de sensiblidad a fármacos.1,2
En su publicación, GLI esbozó un algoritmo de preferencia para promover el acceso universal de los pacientes a pruebas rápidas de la resistencia a la tuberculosis y a la rifampicina.1 Para obtener más información sobre el modelo de GLI, haga clic aquí.

1. Global Laboratory Initiative. Algoritmos de diagnóstico para TB con el modelo GLI. Acceso: marzo de 2017. http://www.stoptb.org/wg/gli/assets/documents/GLI_algorithms.pdf
2. European Tuberculosis Laboratory Initiative. Algoritmo para el diagnóstico de laboratorio y la monitorización del tratamiento de la tuberculosis pulmonar y la tuberculosis resistente a fármacos mediante tecnologías de diagnóstico molecular rápido de última generación. Acceso: marzo de 2017. http://www.euro.who.int/__data/assets/pdf_file/0006/333960/ELI-Algorithm.pdf
Las complejas vías de transmisión del ERV requieren un cribado activo
Un estudio de 7 años de duración sobre las vías de transmisión hospitalaria de Enterococcus resistentes a vancomicina (ERV) realizado en un solo instituto de Cambridge, Reino Unido, proporciona información nueva con importantes repercusiones para el control de infecciones hospitalarias. El estudio identificó varias rutas de introducción de ERV en el hospital, seguidas de una compleja red de transmisión posterior del microorganismo.
Estos hallazgos refuerzan la importancia de realizar un cribado activo para detectar a los portadores de ERV en combinación con medidas de control de infecciones para evitar que continúe la transmisión. Como parte de un programa más amplio de prevención de infecciones, el cribado activo puede reducir las tasas de colonización e infección por ERV, lo que puede dar lugar a tasas más bajas de infección como las observadas en países que aplican esta estrategia, como Finlandia y los Países Bajos.
En este estudio se utilizaron datos de ingreso y movimiento de pacientes en la planta, junto con métodos avanzados de secuenciación del genoma completo para realizar un seguimiento de la introducción y transmisión de varias cepas de ERV. Más del 50 % de los aislados encontrados en el estudio estaban estrechamente relacionados al menos con otro aislado, lo que destaca la complejidad de la transmisión de ERV dentro del hospital. A partir de los datos, los investigadores concluyeron que las intervenciones centradas en el control de infecciones a raíz únicamente de la investigación de brotes, sin un cribado activo, solo son parcialmente eficaces para reducir las tasas de ERV.
El cribado activo reduce las tasas de infección por ERV, y los países que implementan esta estrategia (como Finlandia y los Países Bajos) tienen tasas de infección por ERV considerablemente más bajas que el Reino Unido».
El ERV es una de las principales causas de infecciones asociadas a la atención sanitaria. Estas infecciones, en comparación con las causadas por enterococos sensibles a vancomicina, tienen mayores tasas de mortalidad y costes sanitarios. Debido a que con frecuencia persisten en los entornos hospitalarios, las cepas de Enterococcus faecium resistentes a vancomicina son especialmente difíciles de erradicar. Esta dificultad aumenta por la falta de un cribado activo.
El informe de los resultados se publicó en Clinical Infectious Diseases.
KE Raven et al. Clinical Infectious Diseases 2017
El siguiente artículo de consenso destaca las ventajas de realizar pruebas de S. aureus antes de la cirugía
En un reciente artículo de consenso, un grupo internacional de expertos en control de infecciones destacó las ventajas de utilizar la tecnología de diagnóstico molecular rápida para la detección de portadores de SARM/S. aureus antes de la cirugía.
Las infecciones de heridas quirúrgicas (IHQ) se encuentran entre las infecciones intrahospitalarias (IIH) más frecuentes y se asocian a una morbimortalidad considerable. La colonización nasal con S. aureus es el factor de riesgo independiente más importante para el desarrollo de una IHQ en una cirugía limpia; y su incidencia es de 2 a 9 veces mayor en portadores que en no portadores.
Tras la primera mesa redonda europea sobre infecciones de heridas quirúrgicas por S. aureus (1st European S. aureus & Surgical Site Infection round table), 10 expertos europeos y americanos revisaron las pruebas científicas del valor de la detección y posterior descolonización preoperatoria de los portadores nasales de S. aureus. Sus hallazgos se publicaron como un artículo de consenso en el Journal of Hospital Infection.
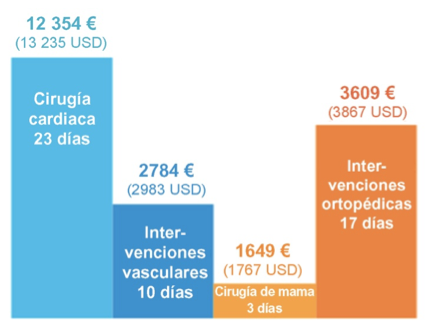
Coste y prolongación de la estancia hospitalaria de las IHQ
Existe una clara correlación entre el uso empírico/universal de mupirocina y antiséptico, y la aparición de resistencia a estos agentes en SASM, SARM y S. epidermidis, que aumenta del 60 % al 95 %.
Una solución eficaz para los pacientes que se someten a una cirugía limpia es el uso de la tecnología de diagnóstico molecular rápida para la identificación preoperatoria de portadores de SASM y SARM, seguida por la descolonización con clorhexidina y mupirocina.
Esta estrategia de tratamiento se asocia a tasas más bajas de IHQ y un menor coste:
- Reducción de un 60% en la tasa de infecciones por S. aureus
- Disminución del 57% en la tasa de mortalidad
- Disminución de 2 días en la estancia hospitalaria
- Reducción del coste de la atención en 2.841 € (3.044 USD) por cada paciente cardiotorácico y en 955 € (1.023 USD) por cada paciente ortopédico
La detección y la descolonización selectiva de los pacientes positivos para S. aureus tienen las ventajas de prevenir las IHQ, ayudar a reducir costes, monitorizar los cambios en los aislados circulantes de SASM y SARM, y minimizar la aparición de resistencia ».
Referencia:
H. Humphreys et al. Journal of Hospital Infection 2016
Carbapenemasas: Experiencias en el Reino Unido
Watch Now
Conozca la opinión de destacados expertos del Reino Unido sobre los recientes retos y soluciones relacionados con las bacterias enterobacteriáceas productoras de carbapenemasas en el noroeste de Inglaterra.
El Reino Unido ha sido pionero en la introducción de métodos innovadores para enfrentarse a la amenaza de las carbapenemasas y limitar la propagación de estos peligrosos microorganismos. Haga clic en las tres imágenes arriba expuestas para escuchar entrevistas cortas con importantes expertos de este campo:
- Dr. Tim Neal – Doctor de Control de Infecciones (Infection Control Doctor), Laboratorios Clínicos de Liverpool (Liverpool Clinical Laboratories)
- Dr. Andrew Dodgson – Jefe de Microbiología y Control de Infecciones (Microbiology and Infection Control Lead), Central Manchester Foundation Trust
- Terry Whalley – Director de estrategia y sostenibilidad – Wirral University Teaching Hospital NHS Foundation Trust
El papel del diagnóstico molecular en la detección sistemática de enterobacterias resistentes a los carbapenems
Watch Now
En la reunión IDWeek 2016 que tuvo lugar en Nueva Orleans, la Dra. Teena Chopra presentó una ponencia titulada «Rapid Diagnostics in the Post Antibiotic Era: Averting a Catastrophe» (Diagnóstico rápido en la era posantibiótica: Evitando una catástrofe). Haga clic en la imagen anterior para ver una reproducción de toda la ponencia.
Este vídeo se suministró con permiso de la ponente.
Limitación de la propagación
MRSA, C. difficile, enterobacteriáceas resistentes al carbapenem, enterococos resistentes a la vancomicina, tuberculosis – Los organismos resistentes a los medicamentos suponen una amenaza mortal, comprometiendo nuestra capacidad para poder atender a los pacientes.1,2 ¿Qué dimensión tiene el peligro y qué medidas inmediatas podemos adoptar antes de que sea demasiado tarde?
La creciente crisis en todo el mundo3

1. Centers for Disease Control and Prevention. “About Antimicrobial Resistance.” Available at http://www.cdc.gov/drugresistance/about.html. Accessed December 21, 2015.;
2. World Health Organization. “Antimicrobial resistance: global report on surveillance.” June, 2014.;
3. “Antibiotic resistance – the global threat.” Available at: http://www.cdc.gov/drugresistance/pdf/antibiotic_resistant_fs.pdf. Accessed December 21, 2015.
Menú integral para la detección rápida y precisa de la resistencia
Los pacientes con infecciones producidas por bacterias resistentes a los medicamentos tienen un mayor riesgo de complicaciones clínicas y de mortalidad, y suelen requerir más recursos sanitarios que los pacientes infectados con bacterias susceptibles.1 La identificación a tiempo y fiable de los patógenos resistentes forma parte integral de un plan de acción para limitar la propagación de la resistencia antimicrobiana.
Nivel de amenaza según los CDC
1. World Health Organization. “Antimicrobial resistance: global report on surveillance.” June, 2014.
Vigilancia activa para reducir las tasas de MRSA y mejorar los resultados
Watch Now
El MRSA es una infección asociada a la atención sanitaria (IAAS) frecuente, que provoca cientos de miles de infecciones a nivel mundial cada año. Por ejemplo, solamente en los Estados Unidos se producen anualmente hasta 375.000 infecciones por MRSA y 23.000 muertes relacionadas.1 La implantación de pruebas PCR a demanda con Xpert MRSA seguido por el aislamiento de los pacientes infectados o colonizados con MRSA ha demostrado reducir las tasas de IAAS y los costes relacionados con la infección.2
Haga clic aquí para obtener más información sobre la integración de pruebas moleculares a demanda en uno de los Programas de Vigilancia Activa del MRSA del hospital.
1. Kavanagh KT, Calderon LE, Saman DM and Abusalem SK. The use of surveillance and preventative measures for methicillin-resistant staphylococcus aureus infections in surgical patients. Antimicrob Resist Infect Control. 2014;3:18. ;
2. Spencer M, Barnes S, Parada J et al. A primer on on-demand polymerase chain reaction technology. Am J Infect Control. 2015;43:1102-8.









