Carbapenemases: Défis et solutions en Europe
Watch Now
Ecoutez le témoignage d’experts sur les défis et solutions concernant les Entérobactéries productrices de carbapénèmases en France et en Italie. Visionnez ci-dessous la vidéo de la brève interview de:
- Thierry Naas – Centre National de Référence des résistances aux antibiotiques
- Gian Maria Rossolini – Hôpital universitaire Careggi et Claudio Macchi – Fondation Don Gnocchi de Florence en Italie
Empêcher les « bactéries hautement résistantes » de provoquer des épidémies catastrophiques
|
Début 2015, le terme Entérobactéries productrices de carbapénémases (EPC) est entré dans le vocabulaire courant à l’occasion d’une épidémie très médiatisée survenue dans un hôpital de Californie. Celle-ci a entraîné deux décès et a été associée à des endoscopes médicaux contaminés1. Pourtant cela fait plus de 10 ans que ces organismes pathogènes multirésistants constituent un problème de plus en plus préoccupant. Les infections par EPC se sont multipliées par 5 entre 2008 et 2012, atteignant 48 États en 20122. D’après les U.S. Centers for Disease Control and Prevention (CDC), environ 4% des hôpitaux de soins de courte durée et 18% des hôpitaux de long séjour américains ont signalé au moins un cas d’infection par EPC au cours du premier semestre 20123. Aujourd’hui, en 2017, une étude intitulée Contrôle des infections et épidémiologie hospitalière portant sur 16 établissements de soins dans la région de Washington, D.C. a révélé un taux de prévalence étonnamment élevé de 5,2%4. Ce n’est qu’une région métropolitaine des États-Unis, mais il ne s’agit certainement pas d’un cas isolé. CLIQUEZ ICI pour télécharger le livre blanc. |
1. Terhune C. Superbug linked to 2 deaths at UCLA hospital; 179 potentially exposed. Los Angeles Times. 2015 Feb 18. Accessed Oct 2017. http://www.latimes.com/business/la-fi-hospital-infections-20150218-story.html
2. Thaden JT, et al. Rising rates of carbapenem-resistant Enterobacteriaceae in community hospitals: a mixed-methods review of epidemiology and microbiology practices in a network of community hospitals in the Southeastern United States. Infect Control Hosp Epidemiol. 2014 Aug;35(8):978-83.
3. CDC. CDC: Action needed now to halt spread of deadly bacteria. Press release. 2013 Mar 5. Accessed Oct 2017. https://www.cdc.gov/media/releases/2013/p0305_deadly_bacteria.html
4. Reuben J, et al; HARP Study Team. Healthcare antibiotic resistance prevalence - DC (HARP-DC): a regional prevalence assessment of carbapenem-resistant Enterobacteriaceae (CRE) in healthcare facilities in Washington, District of Columbia. Infect Control Hosp Epidemiol. 2017 Aug;38(8):921-29.
Tests moléculaires de routine pour la surveillance des EPC dans un contexte de faible prévalence
Une étude a évalué des patients à haut risque d’être porteurs d’Entérobacteries productrices de carbapénémases (EPC) et a démontré que la surveillance de routine peut orienter efficacement les programmes de contrôle des infections afin de limiter la dissémination des EPC, même dans des régions de faible prévalence.
La détection précoce des patients colonisés par des EPC est essentielle pour le contrôle des infections, mais il n’existe aucune recommandation précise sur quand utiliser les méthodes moléculaires pour la surveillance active dans les contextes de prévalence faible. Cette étude a démontré qu’un test moléculaire rapide est bien adapté à la surveillance de routine des patients à haut risque, même dans les régions de faible prévalence : il a été démontré que le test de Cepheid Xpert® Carba-R a une sensibilité de 100 % et une spécificité de 99,13 % pour la détection des EPC à partir d’écouvillons rectaux par rapport à une culture sur milieu chromogène après enrichissement.
L’étude a été menée dans un hôpital français où la prévalence des EPC est < 1 %. Les « patients à haut risque » comprenaient les rapatriés de pays connus pour présenter une prévalence élevée d’EPC et les patients contacts d’un porteur connu d’EPC. L’étude a permis de regrouper des porteurs, ce qui est essentiel (i) pour prévenir les épidémies et (ii) pour réduire l’impact social. De plus, les patients à haut risque d’EPC négatifs n’ont pas à subir des mesures d’hygiène inutiles entraînant des coûts supplémentaires.
Le rapport des observations a été publié dans International Journal of Antimicrobial Agents.
Cette étude a démontré que le test Xpert® Carba-R est bien adapté à la surveillance rapide des patients à haut risque même dans des régions de faible prévalence »
Référence:
Hoyos-Mallecot et al. Int J Antimicrob Agents 49 (6), 774-777. 2017 Apr 12.
Protocole développé par le Global Laboratory Initiative visant la détection précoce des cas de tuberculose active
Les laboratoires jouent un rôle essentiel dans l’identification précoce des cas de tuberculose active (TB), qui est un facteur clé pour l’élimination de cette maladie à l’échelle mondiale. Afin de répondre aux objectifs de l’OMS pour la prévention de la transmission de la tuberculose et l’amélioration des soins aux patients, le dépistage rapide des sujets avec suspicion de tuberculose à l’aide de tests de diagnostic moléculaire sensibles est recommandé par le Global Laboratory Initiative (GLI) et le European Tuberculosis Laboratory Initiative (région européenne de l’OMS). Ces deux groupes d’experts internationaux recommandent l’utilisation du test Cepheid Xpert MTB/RIF comme test de première intention, plutôt que l’examen microscopique de frottis ou la technique LIPA (Line Probe Assay) en association avec des méthodes de culture cellulaire pour les tests de sensibilité aux antibiotiques.1,2
Dans son article, la GLI a ébauché un algorithme préférentiel pour promouvoir l’accès universel des patients aux tests rapides pour la détection de la tuberculose et la résistance à la rifampicine.1 Pour en savoir plus sur le modèle de la GLI, cliquez ici.

1. Global Laboratory Initiative. GLI model TB diagnostic algorithms. Consulté en mars 2017. http://www.stoptb.org/wg/gli/assets/documents/GLI_algorithms.pdf
2. European Tuberculosis Laboratory Initiative. Algorithm for laboratory diagnosis and treatment-monitoring of pulmonary tuberculosis and drug-resistant tuberculosis using state-of-the-art rapid molecular diagnostic technologies. Consulté en mars 2017. http://www.euro.who.int/__data/assets/pdf_file/0006/333960/ELI-Algorithm.pdf
Les voies de transmission complexes des entérocoques résistants à la vancomycine nécessitent un dépistage actif
Une étude sur 7 ans sur les voies de transmission nosocomiale des entérocoques résistants à la vancomycine (ERV) dans un institut de Cambridge, au Royaume-Uni, offre de nouvelles informations avec des implications importantes pour la lutte contre les infections hospitalières. L’étude a identifié plusieurs voies d’introduction des ERV dans l’hôpital ainsi qu’un réseau complexe de transmission des micro-organismes par la suite.
Ces résultats renforcent l’importance d’un dépistage actif afin de détecter les porteurs d’ERV en conjonction avec des mesures de lutte contre les infections pour éviter d’autres transmissions. Dans le cadre d’un programme de prévention des infections plus large, le dépistage actif peut réduire les taux de colonisation et d’infection par les ERV, ce qui peut entraîner des taux d’infection plus bas similaires à ceux des pays ayant mis en place cette stratégie, comme la Finlande et les Pays-Bas.
Cette étude a utilisé des données issues des admissions de patients et des déplacements dans les services hospitaliers ainsi que des méthodes de séquençage avancé du génome entier pour suivre l’introduction et la transmission de plusieurs souches d’ERV. Plus de 50 % des souches trouvées dans l’étude étaient très proches d’au moins une autre souche, ce qui met en évidence la complexité de la transmission des ERV au sein de l’hôpital. Grâce à ces données, les investigateurs ont conclu que les interventions ciblées de lutte contre les infections qui sont déclenchées uniquement par les investigations de flambées épidémiques, sans dépistage actif, ne seraient que partiellement efficaces dans la réduction des taux d’ERV.
Le dépistage actif réduit les taux d’infection par les ERV et les pays qui ont mis en place cette stratégie (comme la Finlande et les Pays-Bas) présentent des taux d’infection par les ERV considérablement plus bas que ceux du Royaume-Uni. »
Les ERV sont l’une des principales causes d’infections nosocomiales. Ces infections, par rapport à celles causées par les entérocoques sensibles à la vancomycine, présentent des taux de mortalité et des coûts de santé plus élevés. Étant donné qu’elles peuvent souvent rester présentes dans l’établissement hospitalier, les souches résistantes à la vancomycine d’Enterococcus faecium représentent un défi particulier quant à leur éradication. Ce problème est amplifié par l’absence de dépistage actif.
Le rapport contenant ces résultats a été publié dans Clinical Infectious Diseases.
KE Raven et al. Clinical Infectious Diseases 2017
Les avantages des tests de dépistage de S. aureus avant intervention chirurgicale sont mis en avant dans un article de consensus
Un groupe international d'experts en matière de lutte contre les infections met en avant les avantages de l’utilisation d’une technologie de diagnostic moléculaire rapide pour le dépistage pré-opératoire des porteurs de SARM/S. aureus dans un article de consensus récent.
Les infections sur site opératoire (ISO) font partie des infections nosocomiales les plus courantes et entraînent une morbidité et une mortalité importantes. La colonisation nasale par S. aureus est le facteur de risque indépendant le plus important pour le développement d’une ISO en chirurgie propre. En effet, le taux est 2 à 9 fois plus élevé chez les porteurs que chez les non porteurs.
Suite à la 1st European S. aureus & Surgical Site Infection round table (1ère table-ronde européenne sur les infections à S. aureus sur site opératoire), 10 experts européens et américains ont analysé les preuves mettant en évidence la valeur du dépistage du portage nasal de S. aureus et de la décolonisation consécutive des patients positifs avant l’intervention. Leurs conclusions ont été publiées sous la forme d’un article de consensus dans le Journal of Hospital Infection.
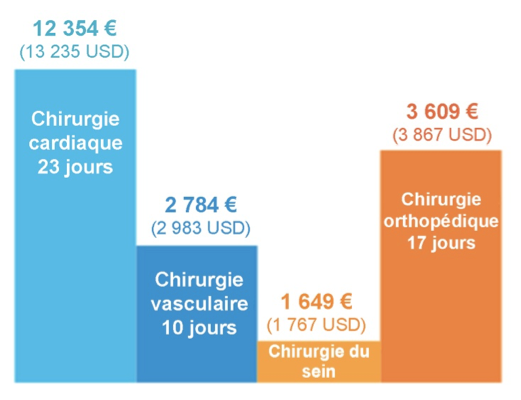
Durée de séjour et coût supplémentaire associés à une ISO
Il existe une nette corrélation entre l’utilisation empirique/universelle de mupirocine et d’antiseptique et l’émergence de la résistance des SASM, SARM et S. epidermidis, pouvant atteindre 60 à 95 %.
L’utilisation d’une technologie de diagnostic moléculaire rapide pour l’identification pré-opératoire des porteurs de SASM et de SARM, suivie d’une décolonisation par mupirocine et chlorhexidine représente une solution efficace pour les patients devant subir une intervention en chirurgie propre.
Cette stratégie de traitement est associée à une réduction des taux d’ISO et à des économies :
- Réduction du taux d’infection par S. aureus de 60%
- Réduction du taux de mortalité de 57%
- Réduction de la durée moyenne de séjour de 2 jours
- Réduction du coût des soins de 2 841 € (3,044 USD) par patient en chirurgie cardio-thoracique et de 955 € (1,023 USD) par patient en chirurgie orthopédique
Le dépistage et la décolonisation sélective de patients positifs à S. aureus offrent les avantages de prévenir les ISO, de contribuer à limiter les coûts, de surveiller les évolutions des souches de SASM et de SARM et de limiter l’émergence de résistances. »
Référence :
H. Humphreys et al. Journal of Hospital Infection 2016
Carbapénémases – Expériences britanniques
En-tête
Écoutez de grands spécialistes du Royaume-Uni s’exprimer sur les enjeux récents des entérobactéries productrices de carbapénémases (EPC) et sur les solutions mises en œuvre dans le Nord-Ouest de l’Angleterre.
Le Royaume-Uni est en tête des approches innovantes visant à lutter contre les carbapénémases et à limiter la propagation de ces organismes dangereux. Cliquez sur les trois images ci-dessus pour écouter de brèves entrevues avec des spécialistes majeurs dans ce domaine :
- Dr. Tim Neal – Médecin spécialiste de la lutte contre les infections (Infection Control Doctor) – Laboratoires cliniques de Liverpool (Liverpool Clinical Laboratories)
- Dr. Andrew Dodgson – Responsable des services de microbiologie et de lutte contre les infections (Microbiology and Infection Control Lead) – Central Manchester Foundation Trust
- Terry Whalley – Directeur de la Stratégie et du Développement Durable – Wirral University Teaching Hospital NHS Foundation Trust
Rôle du diagnostic moléculaire dans le dépistage des ERC
En-tête
Lors de la réunion IDWeek de 2016 à la Nouvelle Orléans, Dr. Teena Chopra a fait une présentation intitulée « Rapid Diagnostics in the Post Antibiotic Era: Averting a Catastrophe. » (Diagnostic rapide dans l’ère post-antibiotique : éviter une catastrophe). Cliquez sur l’image ci-dessus pour visionner une retransmission de la présentation complète.
Cette vidéo a été mise à disposition avec l’autorisation de l’oratrice.
Limiter la propagation
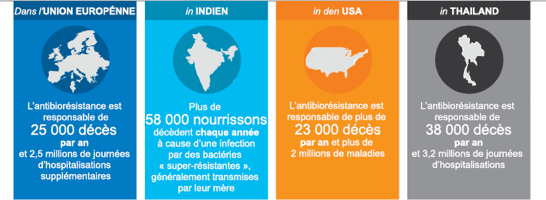
SARM, C. difficile, entérobactéries résistantes aux carbapénèmes, entérocoques résistant à la vancomycine, tuberculose — Les microorganismes pharmacorésistants constituent une menace mortelle pour notre capacité à prendre en charge les patients.1,2 Quelle est l’importance du danger, et quelles mesures immédiates pouvons-nous prendre avant qu’il ne soit trop tard?
Un problème mondial en augmentation3
1. Centers for Disease Control and Prevention. “About Antimicrobial Resistance.” Available at http://www.cdc.gov/drugresistance/about.html. Accessed December 21, 2015.;
2. World Health Organization. “Antimicrobial resistance: global report on surveillance.” June, 2014.;
3. “Antibiotic resistance – the global threat.” Available at: http://www.cdc.gov/drugresistance/pdf/antibiotic_resistant_fs.pdf. Accessed December 21, 2015.
Menu complet pour une détection rapide et précise de la résistance
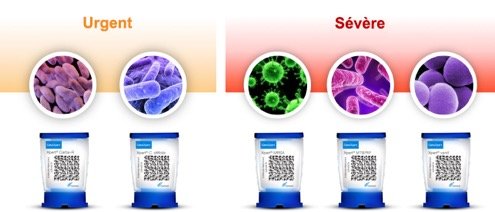
Les patients souffrant d’infections dues à des bactéries pharmacorésistantes présentent un risque supérieur d’aggravation de l’évolution clinique et de mortalité, et consomment souvent plus de ressources sanitaires que les patients infectés par des bactéries sensibles aux médicaments.1 L’identification rapide et fiable des pathogènes pharmacorésistants est essentielle pour limiter la propagation de la résistance antimicrobienne.
Niveau d’alerte du CDC
1. World Health Organization. “Antimicrobial resistance: global report on surveillance.” June, 2014.
Surveillance active pour réduire la prévalence du SARM et améliorer les résultats
Watch Now
Le SARM est souvent responsable d’infections nosocomiales, provoquant des centaines de milliers d’infections dans le monde chaque année. Par exemple, jusqu’à 375 000 infections à SARM et 23 000 décès surviennent chaque année aux seuls États-Unis.1 Il a été montré que l’implémentation du test PCR à la demande Xpert MRSA, suivie de l’isolement des patients infectés ou colonisés par le SARM, permet de réduire les taux d’infections nosocomiales ainsi que les coûts liés à ces infections.2
Cliquez ici pour en savoir plus sur l’intégration des tests moléculaires à la demande dans le programme de surveillance active du SARM d’un hôpital.
1. Kavanagh KT, Calderon LE, Saman DM and Abusalem SK. The use of surveillance and preventative measures for methicillin-resistant staphylococcus aureus infections in surgical patients. Antimicrob Resist Infect Control. 2014;3:18. ;
2. Spencer M, Barnes S, Parada J et al. A primer on on-demand polymerase chain reaction technology. Am J Infect Control. 2015;43:1102-8.









